Hmota je výrazem pro veškeré fyzikálně zachytitelné formy objektivní reality, tedy toho, co existuje nezávisle na našem vědomí, a projevy čehož lze objektivně zaznamenat či změřit. Dle současného pohledu kvantové fyziky se veškerá známá hmota ve vesmíru skládá z tzv. elementárních částic (šesti druhů kvarků a šesti druhů leptonů) a všechny jevy, které ve vesmíru pozorujeme, dovedeme vysvětlit pomocí čtyř druhů tzv. základních interakcí: gravitační, elektromagnetické, silné a slabé.
Působení každé z těchto sil je zprostředkováno některým z fyzikálních polí. Pole posledních dvou jmenovaných sil, slabé a silné interakce, je omezeno jen na vnitřek atomů a přímo se v makrosvětě neuplatňuje. V něm se uplatňuje elektromagnetismus a gravitace. V měřítku, ve kterém se budeme v tomto článku pohybovat, můžeme uvažovat působení pouze elektromagnetických sil.
Atom, nejmenší, chemicky nedělitelná částice běžné hmoty, se skládá z jádra tvořeného neutrony a protony (kvarky) a elektronového obalu okolo se pohybujících elektronů (lepton). Zastoupení jednotlivých částic bývá většinou ve stejném poměru. Chemické prvky, jak je známe, jsou atomy s rozdílným počtem těchto elementárních částic, přičemž neutrony s protony jsou vždy sdružené v jádře, zatímco elektrony obíhají okolo jádra v jednotlivých vrstvách, tzv. orbitalech. Orbitaly popisují oblasti výskytu elektronů, každý má svůj charakteristický soustředný tvar a každý pojme určitý počet elektronů. Právě zbývající počet elektronů v nezaplněném vnějším orbitalu je to, co určuje fyzikálně chemické vlastnosti daného prvku a také způsob vytváření vazeb mezi nimi. Počet prázdných míst v orbitalu určuje tzv. elektronegativitu neboli schopnost atomu přitahovat přebývající elektrony jiného atomu.
Vytvořením chemické vazby mezi dvěma a více atomy vznikne molekula. Tento děj, jako každý ve vesmíru, musí probíhat po energetickém spádu, tzn., že celková energie vzniklé sloučeniny je nižší než součet energií jejích samostatných členů. V rámci takových vazeb mohou být elektrony nezaplněných orbitalů sdíleny či předány, přičemž struktura orbitalů a hustota elektronů v nich je změněna. V případě vzniku molekuly nabývají orbitaly původně středově souměrných atomů různé tvary a dochází k redistribuci elektronů do tzv. molekulových orbitalů rozprostřených přes atomová jádra sloučeniny – viz obrázek 1, kde je znázorněn vznik molekuly vody ze dvou atomů vodíku (H) a jednoho atomu kyslíku (O). Spojené atomy k sobě vznikem vazby zaujmou prostorovou orientaci danou jejich velikostí (více elektronů se soustředí u většího kladně nabitého jádra) a počtem vazebných elektronů. Ve většině případů není sdílení elektronů rovnocenné a molekula se tak stává prostorově i elektricky asymetrickou, tzv. polární.
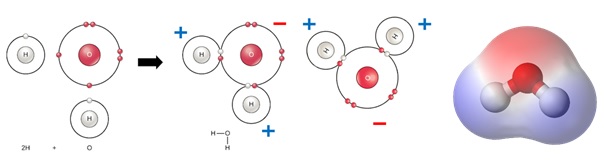
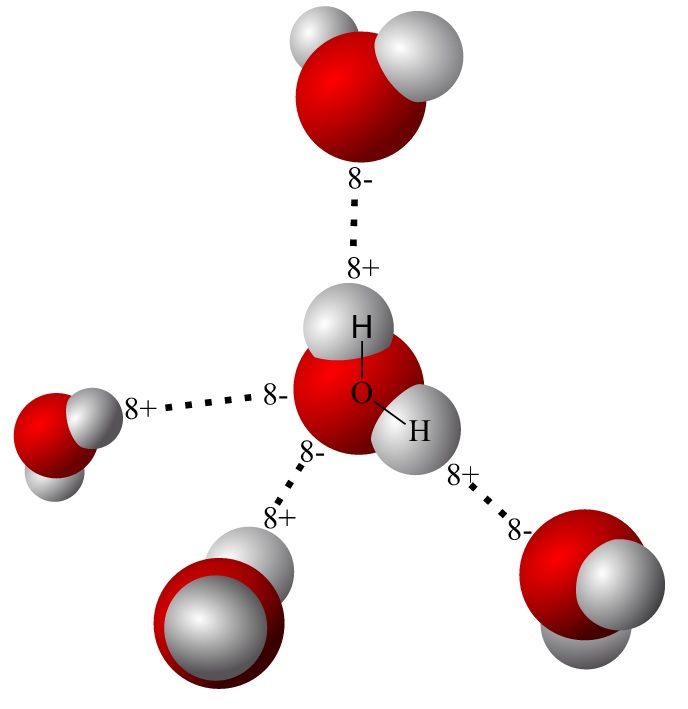
Polární molekula má tedy sama o sobě jistý elektrický náboj, vytvářející elektromagnetické pole kolem ní. Pole opačných nábojů se k sobě navzájem přitahují (tzv. elektrostatické síly) a drží molekuly při sobě, aniž by navzájem sdílely své elektrony. Byť jsou tyto síly poměrně slabé, odpovídají při svém součtu např. za to, že při sobě drží molekuly vody (jak je vidět na obrázku 2) a voda se tak jeví jako kapalina. Nepolární sloučeniny se s polárními neslučují (např. olej ve vodě).
Pro existenci života jsou zapotřebí obrovské molekuly složené z až tisíců atomů, tzv. biopolymery, a to bílkoviny (neboli proteiny), nukleonové kyseliny (DNA) a polysacharidy (např. celulóza). Základní materiál pro stavbu buněk a veškeré jejich funkce jsou proteiny. Přestože jich existuje obrovské množství, jsou všechny složené z pouze dvaceti základních stavebních kamenů, tzv. aminokyselin. Molekuly aminokyselin se spolu spojují chemickými vazbami v pořadí kódovaném genem (DNA) za vzniku proteinu s charakteristickou strukturou a funkcí. Má-li se protein ve výkonu své funkce spojit s nějakým chemickým „partnerem“, musí mít pro toto setkání patřičné vazebné místo. To znamená, že reliéf povrchu obou partnerů do sebe musí přesně zapadnout jak strukturou, tak elektrostatickými poli jako zámek do klíče. Toto spojení musí opět proběhnout po energetickém koncentračním spádu a je definováno tzv. afinitou, která určuje míru vzájemné přitažlivosti mezi partnery. Protein po vzájemném spojení pozmění svůj tvar (tzv. konformační změna), což často přímo či nepřímo vede k vykonání jeho funkce.
Další podmínkou existence života je schopnost reagovat na vnější prostředí. Aby toho byly buňky schopny, jsou obdařeny tzv. receptory, které spouští odpověď uvnitř buňky po navázání specifické molekuly (tzv. ligandu). Ligandem může být jakákoliv molekula mající afinitu k receptoru. Vyšší mnohobuněčné organismy musí být schopny integrovat odpovědi i v rámci svého těla. Pro komunikaci na dálku používají např. hormony nebo v mezineuronové komunikaci tzv. neurotransmitery. Příkladem neurotransmiteru může být serotonin (5-hydroxytryptamin, 5-HT), hrající roli ve smyslovém vnímání, chování, jako je agrese, chuť k jídlu, sex, spánek, nálada, kognice, paměť a další. Pro serotonin existuje v lidském těle 14 specifických receptorů. Každý z nich se nachází v jiných oblastech mozku a spouští jinou odpověď. Je tedy zřejmé, že receptory byly v průběhu evoluce vytvořeny tak, aby byly specifické jak pro svůj ligand, tak pro svou odpověď.
Žádný receptor ovšem není natolik specifický, aby se na něj mohl vázat např. jenom serotonin. Mnoho serotoninu podobných molekul vykazuje afinitu k 5-HT receptoru a úspěšně se s ním váže. Takovými látkami mohou být např. sloučeniny kyseliny lysergové, jako je LSD, nebo ergotamin. Záhadou ovšem zůstává, proč jedna z nich vyvolává tak převratné změny psychiky, zatímco druhá nikoliv i přesto, že se obě látky vážou s podobnou afinitou ke stejným receptorům. Na tuto otázku se již pokoušelo odpovědět několik vědců, žádní však prozatím úspěšně.
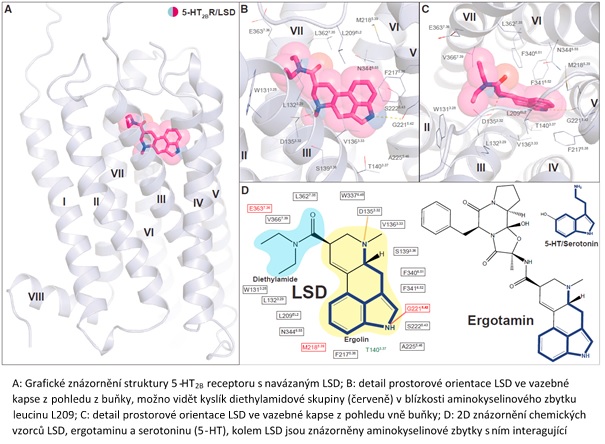
V lednu tohoto roku vyšla publikace nabízející možné vysvětlení. V této studii byla pomocí rentgenové krystalografie stanovena 3D struktura 5-HT2B a 5-HT2A receptorů, které jsou zodpovědné za psychoaktivní účinky LSD. Počítačovými simulacemi molekulární dynamiky proteinu bylo poté zjištěno, že LSD a ergotamin zapadají do „vazebné kapsy“ receptoru jiným způsobem. LSD se váže o něco výš a interaguje s jinými aminokyselinami vnitřní části receptoru. Receptor tak v odpovědi na spojení s molekulou pozmění svůj tvar v každém případě jiným způsobem. Právě konformační změna receptoru je to, co udává interpretaci signálu v buňce a spouští tzv. signalizační kaskádu. Zdá se tedy, že tento nepatrný rozdíl v elektrostatickém působení látek na receptor spouští v každém případě jiné signalizační kaskády, které následně mají na svědomí tak odlišnou odpověď jak na úrovni buněk, tak celého nervového systému. Dalším výsledkem studie bylo stanovení tzv. disociační konstanty, která v podstatě vyjadřuje, že LSD „sedí“ na receptoru po velmi dlouhou dobu. Za tuto skutečnost se ukázal být zodpovědný výběžek receptoru nazvaný EL2 složený ze sedmi aminokyselin. L209 (209. aminokyselina v pořadí od N-konce proteinu – leucin) elektrostaticky interaguje s kyslíkem diethylamidového zbytku LSD a působí tak jako závora bránící LSD utéci z vazebného místa, viz obrázek 3. To z části vysvětluje dobu, po kterou LSD účinkuje.
Veškeré procesy v buňce jsou zpětnovazebně kontrolovány, aby probíhaly ve stálé rovnováze. To platí i pro receptory, které, mají-li navázaný ligand, podněcují přenos signálu a může tak dojít k narušení rovnováhy. Ukončení přenosu bývá uskutečňováno inaktivací receptoru, v některých případech je receptor dokonce pohlcen z membrány dovnitř buňky. Takové chování vykazují i serotoninové receptory. K vysvětlení délky působení LSD přispěla i studie z roku 2014, v níž bylo fosfoproteomickou kvantitativní analýzou zjištěno, že ze všech fosforylací* indukovaných navázáním ligandu na receptor je to právě fosforylace na serinu 280 (orientovaný dovnitř buňky), která může za odlišnou inaktivaci receptoru. V normálním případě (po navázání serotoninu) k této fosforylaci dochází, což je signálem pro tzv. β-arrestin, který spouští výstavbu molekulárního lešení vedoucího k pohlcení receptoru dovnitř buňky. V případě navázání LSD k tomu nedochází a receptor je tak nadále vystaven na buněčné membráně a podněcuje přenos signálu.
Z uvedených studií je tedy zřejmé, že strkáme-li klíče lišící se byť jenom jedním zubem do jednoho zámku, můžeme otevřít úplně jiné dveře.
Čestmír Vejmola
Česká psychedelická společnost
*Pojem fosforylace vyjadřuje adici fosforečné skupiny nejčastěji na –OH skupinu aminokyseliny (serinu, threoninu, nebo tyrosinu). Fosforylace většinou vede ke konformační změně proteinu, čímž dochází k pozměnění jeho funkce. Některé proteiny přechází fosforylací do aktivního stavu, jiné jsou inhibovány.
Literatura:
(1) Wacker D, Wang S, Mccorvy JD, Shoichet BK, Dror RO, Roth BL. Crystal Structure of an LSD-Bound Human Serotonin Receptor. Cell. 2017;168(3):377-389.e12. doi:10.1016/j.cell.2016.12.033.
(2)Karaki S, Becamel C, Murat S, et al. Quantitative Phosphoproteomics Unravels Biased Phosphorylation of Serotonin 2A Receptor at Ser280 by Hallucinogenic versus Nonhallucinogenic Agonists. Mol Cell Proteomics. 2014;13(5):1273-1285. doi:10.1074/mcp.M113.036558.
